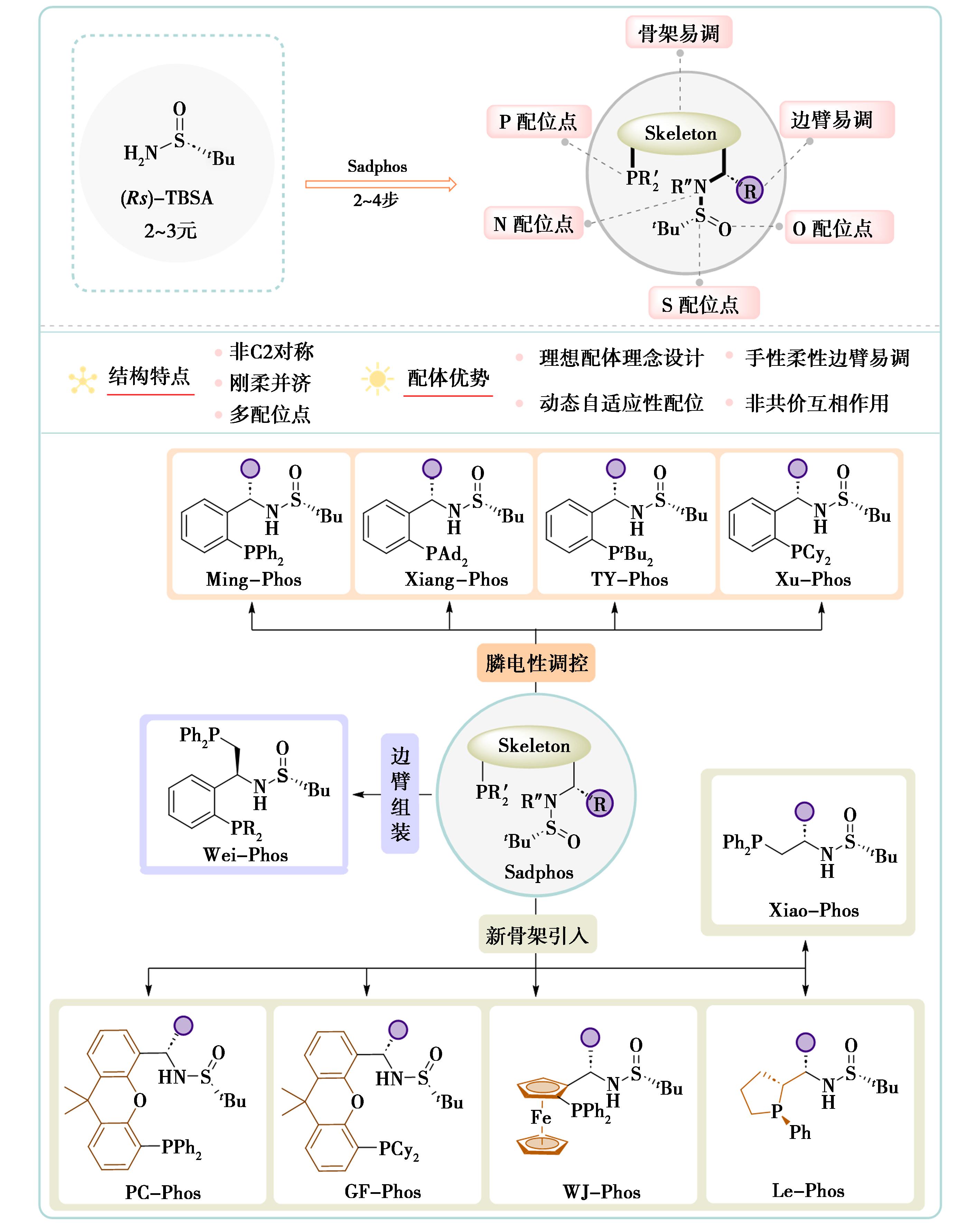
图1 基于“理想”配体设计理念开发的新一代自适应型手性配体/催化剂Sadphos[5]
Fig.1 New generation adaptive chiral ligands/catalysts Sadphos based on the “IDEAL” ligand design concept[5]
手性功能分子与人类生活密切相关,其高效制备依赖于不对称催化技术的突破。近年来,该领域的核心挑战在于发展原创的手性催化剂[1-3]。其中,膦配体作为目前为止研究最多、应用最广泛的配体类型,近半个世纪以来,基于碳骨架的多样性、效果独特性等特点,目前已开发了丰富多样的中心手性、轴手性、面手性、螺环等骨架的手性膦配体,并在不对称催化中取得了系列重要的研究成果[4]。然而,“理想(IDEAL:Inexpensive,Diverse,Easy,Available,Large)配体”的设计开发,一直是合成化学家和工业界共同追求的目标。根据近些年的发展,“理想”配体应具有五大特征:1)廉价原料(Inexpensive);2)丰富的调控位点(Diverse);3)易于合成(Easy);4)利用易得手性试剂(Avaliable);5)适用于大量的反应(Large)。基于“理想配体”设计理念,2014年,首类新一代动态自适应型手性亚磺酰胺膦配体(Sulfinamide Phosphine)Sadphos家族配体Ming-Phos问世(图1)[5]。随后,为更进一步系统研究Sadphos配体的催化活性、化学选择性和立体选择性控制能力[6]。

图1 基于“理想”配体设计理念开发的新一代自适应型手性配体/催化剂Sadphos[5]
Fig.1 New generation adaptive chiral ligands/catalysts Sadphos based on the “IDEAL” ligand design concept[5]
通过电性调节,改变配体膦原子的电负性和配体空间位阻,Xiang-Phos[7]、Xu-Phos[8]、TY-Phos[9]依次被报道;通过骨架调节,改变配体配位基团的键角和配体骨架的刚性,Xiao-Phos[10]、PC-Phos[11]、WJ-Phos[12]、Le-Phos[13]和GF-Phos[14]先后被开发;通过边臂组装,引入二苯基甲基膦,开发了一类手性叔丁基亚磺酰胺双膦配体和多功能有机膦催化剂Wei-Phos[15]。
PC-Phos作为首类优势配体骨架衍生的 Sadphos家族成员,其设计灵感来源于宽螯合角度的经典非手性双膦配体Xantphos[16]。该配体迄今为止已应用于超过2000种过渡金属催化的反应中,并衍生出了Homoxantphos、Sixantphos、Phosxantphos、Thixantphos、Isopropxantphos、Nixantphos、Benzoxantphos、tBu-xantphos以及MePh-xantphos等系列氧杂蒽骨架的非手性双膦配体以及氧杂蒽骨架的膦手性配体[17]。作为基于氧杂蒽骨架最成功的手性配体,PC-Phos在参与反应时表现出了优异的催化活性、化学选择性和立体选择性控制能力。接下来,将按时间的先后顺序并结合反应类型,系统阐述PC-Phos配体在不对称催化反应中的进展。
金催化的官能团化的联烯分子内环化反应作为一种最强大和最直接的合成工具用来原子经济性的构筑环状分子骨架。尽管金(Ⅰ)催化的分子间的联烯胺的环加成反应取得了很大的进展,分子内高选择性的不对称环化依然是一个挑战性的课题。2017年,本课题组首次开发了一种不对称Au(Ⅰ)/PC-Phos催化的分子内联烯胺Pictet-Spengler环化反应,模块化合成了一系列手性四氢咔啉,并将其应用于天然产物(R)-Deplancheine、Desbromoarborescidine A和Desbromoarborescidine C等核心中间体的合成(图2)[11]。该策略解决以下挑战:抑制分子间联烯胺的二聚化且促进分子内环化;控制吲哚在C2位而非C3位反应以及联烯胺在α-位而非γ-位反应。根据产物结构和配体构型,提出了可能的不对称诱导模型:底物磺酰基O与催化剂氮氢形成氢键,配体的4-甲氧基苯基作为手性柔性边臂,屏蔽了联烯的Si面,吲哚从Re面进攻形成高对映选择性产物。
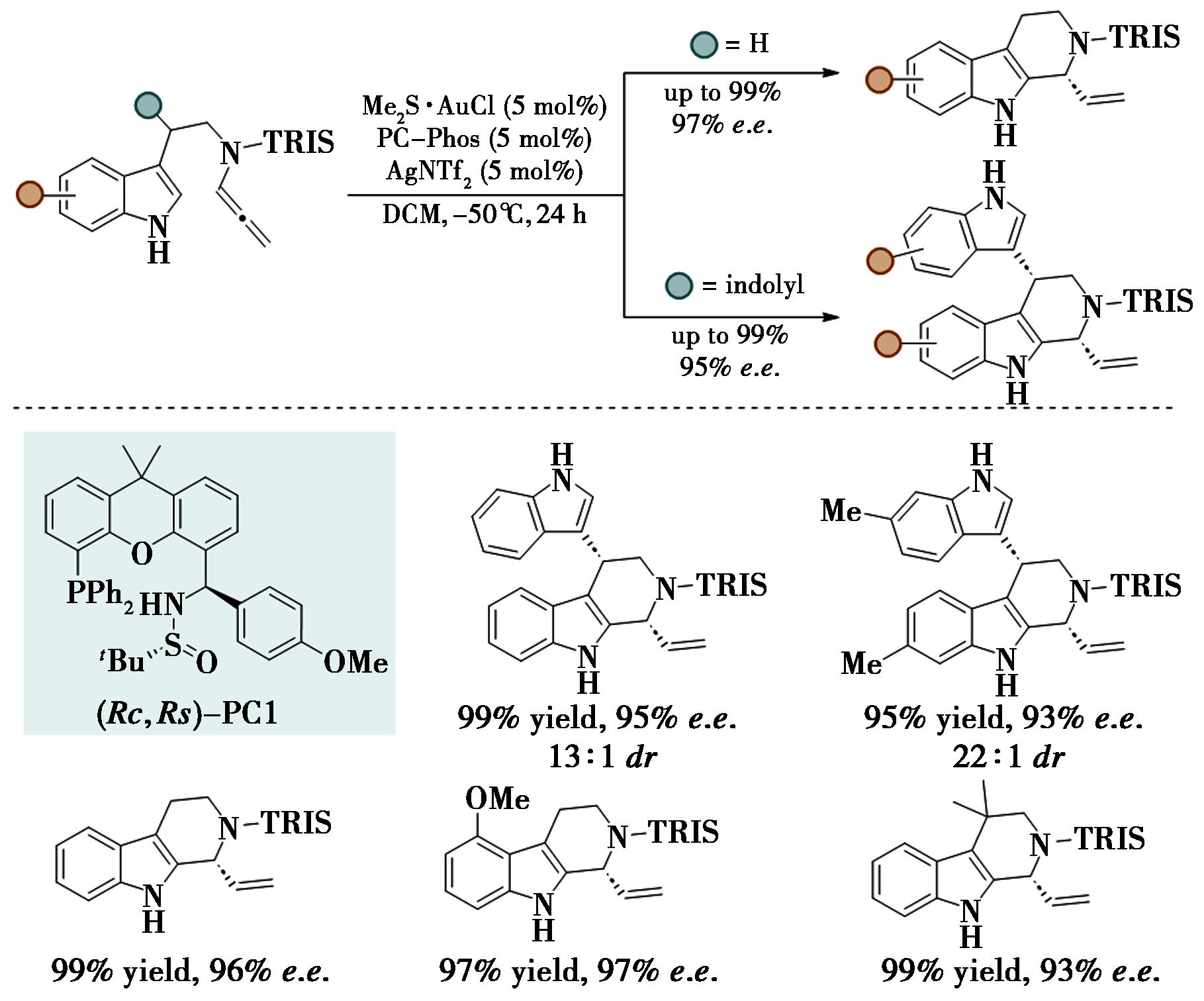
图2 Au/PC-Phos催化的分子内联烯胺参与的不对称Pictet-Spengler反应合成手性四氢咔啉类化合物[11]
Fig.2 Gold/PC-Phos-catalyzed asymmetric Pictet-Spengler of N-allenamides for the synthesis of chiral tetrahydrocarbolines[11]
手性亚砜在天然产物、药物化学(如埃索美拉唑、莫达非尼)及不对称合成中应用广泛,是重要的手性助剂、配体和有机催化剂。传统合成方法存在局限性:亲核取代法依赖高活性锂或镁基亲核试剂,官能团耐受性差;金属催化不对称氧化法面临强氧化剂限制官能团兼容性及过度氧化为砜的问题。因此,开发高效、通用的手性亚砜不对称合成方法极具价值。此前研究存在对映选择性低、底物范围有限等问题,缺乏能同时适用于烷基和芳基亚磺酸根阴离子的通用催化体系。2018年,本课题组报道了Pd/PC-Phos催化对映选择性芳基化合成手性二芳基亚砜;同时解决了烷基次磺酸阴离子芳基化手性转化较低的难题(图3)[18]。Pd/PC-Phos催化对映选择性芳基化合成手性亚砜,也是目前最好的催化体系。该方法能够进一步应用于Sulindac的手性合成。单晶衍射表明,PC-Phos配体通过O,P-原子与钯(Ⅱ)中心形成罕见的十一元环结构,这也是Sadphos家族配体首次应用于钯催化的反应。
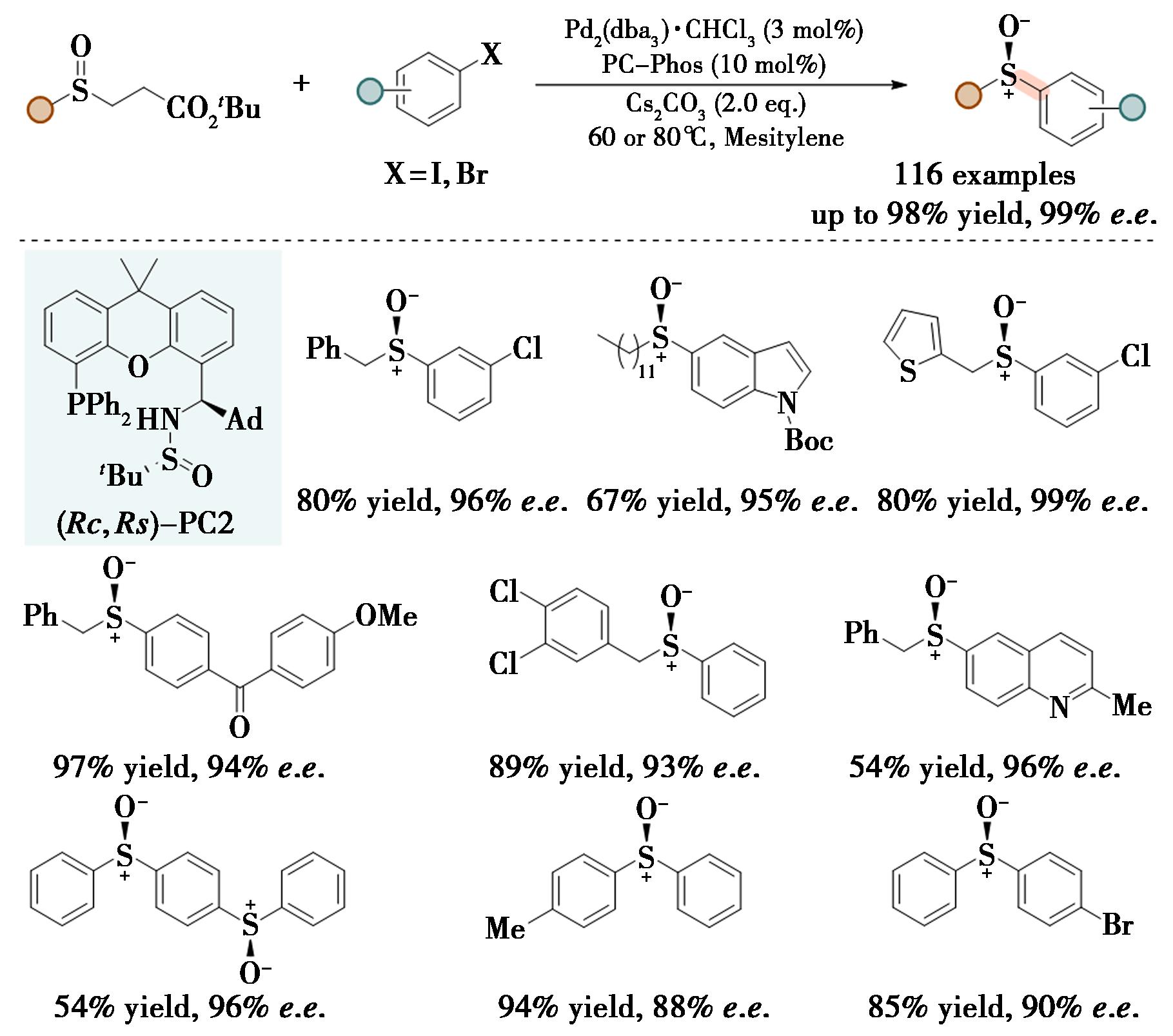
图3 Pd/PC-Phos催化的通用亚磺酸盐阴离子的对映选择性芳基化[18]
Fig.3 Palladium/PC-Phos-catalyzed enantioselective arylation of general sulfenate anions[18]
α-手性烷基磷化合物因具备生物活性及作为手性配体/催化剂的潜力而备受关注。然而,传统合成方法依赖手性助剂和多步骤反应,存在效率低的问题;现有不对称氢化、C—P键偶联等方法也存在局限。其中,苯乙烯的不对称氢磷酸化因底物活性低、区域选择性难控、氢磷酸化合物易互变异构导致催化剂失活等问题,一直是合成领域的挑战。2025年,本课题组开发了一种由PC-Phos配体调控的钯催化苯乙烯的不对称氢磷酸化反应,区域发散性和对映选择性合成手性烷基磷化合物(图4)[19]。实验结果表明,配体的选择对反应的区域选择性和对映选择性具有决定性影响,PC3主要生成马氏产物,rac-BINAP配体则主要生成反马氏产物。通过调整PC-Phos配体的结构,2-叔丁基苯基作为手性柔性边臂,在反应中表现出最佳的活性和对映选择性,通过使用PC3配体的非对映异构体,也可高效制备产物的对映体。该反应对多种带有不同取代基的苯乙烯底物具有良好的耐受性,包括带有电子供体和电子受体的底物,都能以良好的产率和高对映选择性得到相应的手性烷基磷化合物。氘代实验和DFT计算表明,迁移插入是对映选择性决定步骤,迁移插入和还原消除共同调控区域选择性。氢膦酸酯与配体间的氢键作用是高选择性的关键因素,配体的叔丁基与苯乙烯的芳香环也存在色散作用。这一方法不仅为合成手性烷基磷化合物提供了一种高效、经济的途径,还深化了对非共价相互作用在配体设计中的理解。
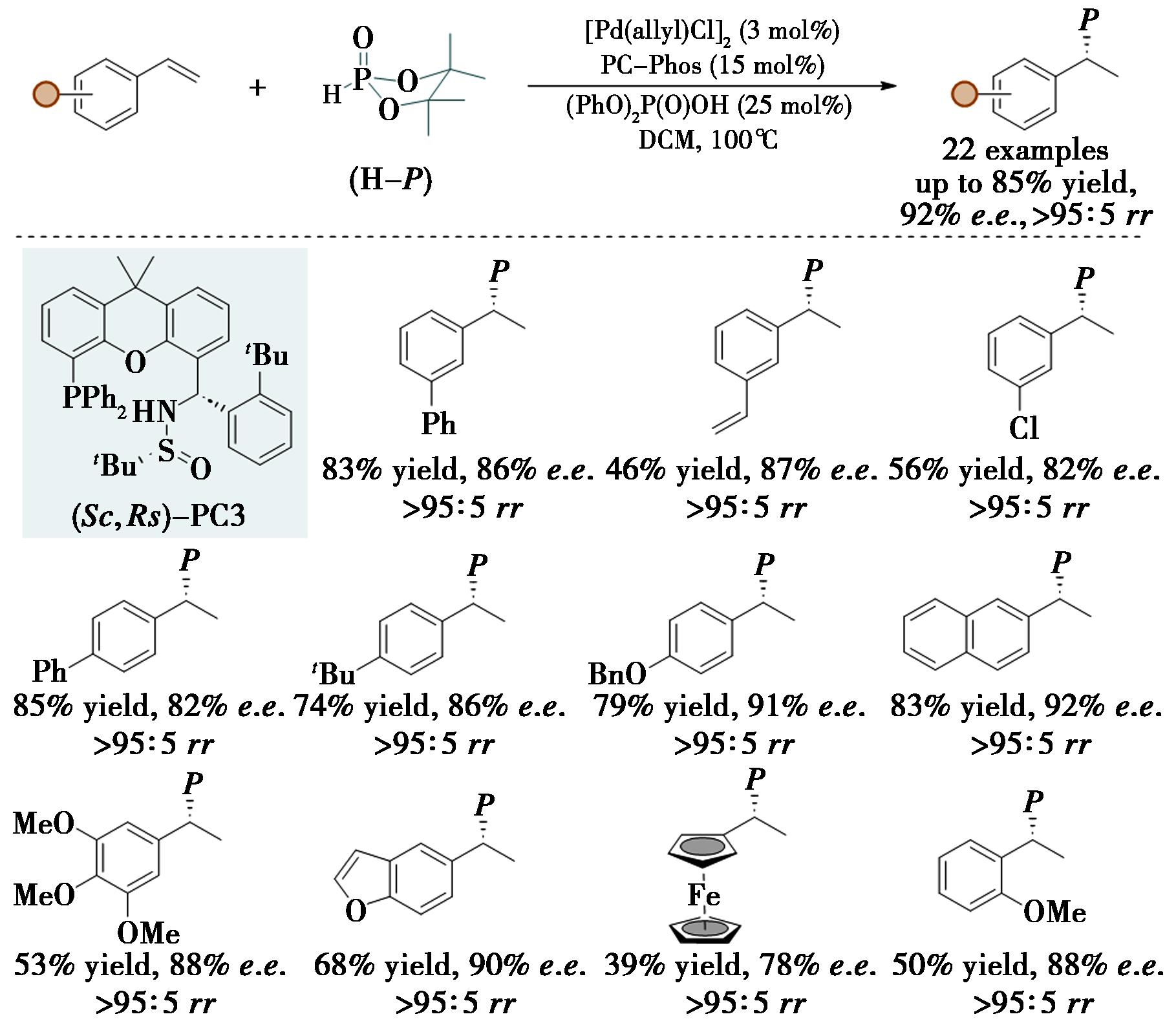
图4 钯/PC-Phos催化的苯乙烯的对映选择性氢磷酸化反应[19]
Fig.4 PC-Phos controlled enantioselective hydrophosphorylation of styrenes by palladium[19]
柱[n]芳烃在生物医学、材料科学和超分子凝胶等领域应用广泛,其中光学纯柱芳烃在手性识别、传感和不对称催化等领域具有重要价值。传统获取手性柱[n]芳烃的方法依赖拆分剂或手性HPLC拆分,通过不对称催化合成此类化合物仍面临挑战。2025年,青岛大学Liu等[20]利用钯催化剂和Sadphos配体,首次开发了一种不对称延伸边臂Suzuki-Miyaura交叉偶联策略,模块化构建了固有手性柱[5]芳烃,避免了传统拆分步骤,产率和选择性显著优于现有方法(图5)。反应核心是通过迭代延伸非手性柱[5]芳烃的取代基,利用边臂空间位阻限制旋转诱导产生固有手性。机理研究表明,第1步Suzuki偶联产物快速外消旋,手性控制主要发生在第2步Suzuki偶联。PC4配体的大位阻柔性边臂与钯中心的空间位阻和电子作用是立体控制的关键。
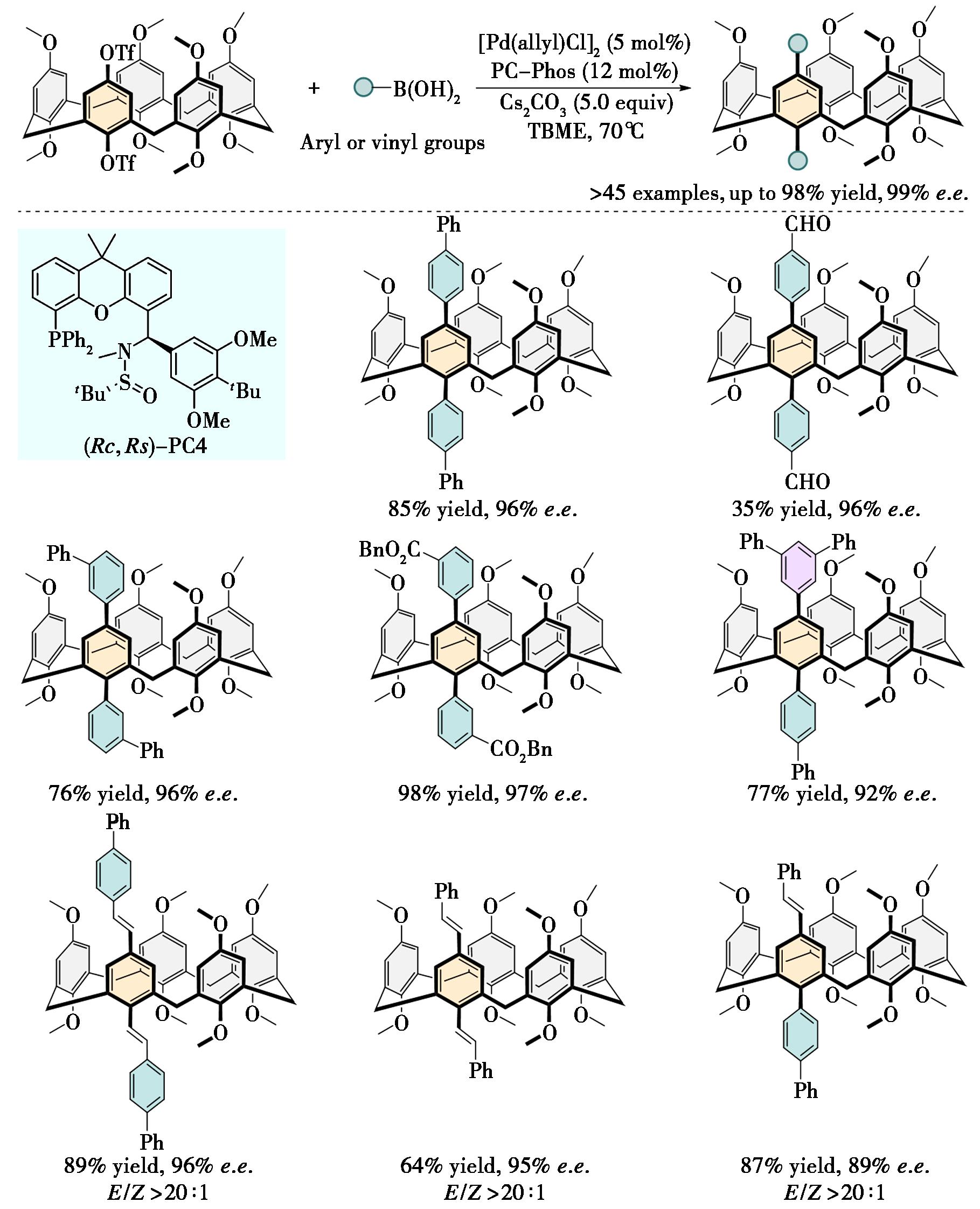
图5 钯/PC-Phos催化的Suzuki-Miyaura偶联反应构建固有手性柱[5]芳烃[20]
Fig.5 Enantioselective construction of inherently chiral pillar[5]arenes via Pd/PC-Phos-catalysed Suzuki-Miyaura cross-coupling[20]
手性螺环戊烷吲哚啉衍生物是一类具有广泛生物活性的重要骨架,在药物化学和天然产物合成中具有重要价值。动态动力学拆分(DKR)是构建富对映体分子的高效策略,可将外消旋体完全转化为目标手性产物。然而,通过吲哚的去芳构化反应实现轴手性到中心手性的立体收敛转化仍面临挑战。2020年,本课题组实现了Pd/PC-Phos催化的吲哚与炔烃的动态动力学拆分的不对称去芳构化反应(DKR/CADA),高效模块化构建了手性螺环化合物,具有操作简便、效率高、对映选择性优异、底物范围广和衍生化多样等特点(图6)[21]。该方法为含手性螺吲哚啉和螺吲哚骨架的生物碱及药物合成提供了新途径,通过控制实验和SAESI-MS对反应中间体的检测发现PC-Phos与Xantphos杂化配位的钯配合物,是促进该反应高对映选择性的活性中间体。
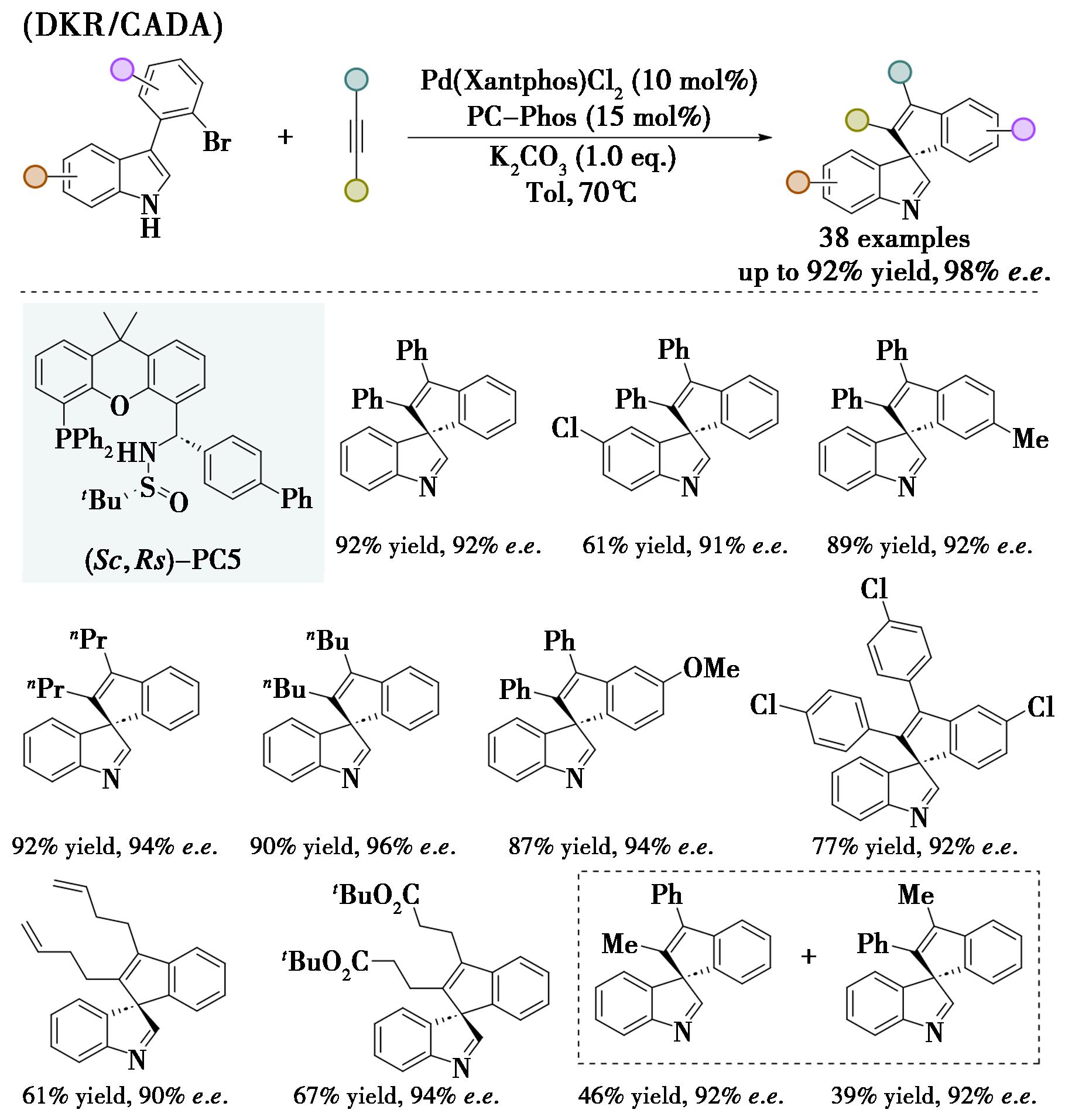
图6 钯/PC-Phos催化的动态动力学拆分实现吲哚的不对称去芳构化[21]
Fig.6 Asymmetric dearomatization of indole via palladium/PC-Phos catalyzed dynamic kinetic transformation[21]
不对称环加成反应是有机化学中构建富含对映体的环状结构的强大工具,在天然产物、药物和农用化学品的对映选择性合成中具有重要意义。然而,与已充分发展的通过钯-三亚甲基甲烷(Pd-TMM)中间体进行的环加成反应相比,杂烯丙基阳离子的杂(3+2)环加成反应极为罕见,主要因其存在轨道对称性不匹配,协同过程禁阻。2022年,本课题组首次实现了亲电性钯-杂烯丙基两性离子中间体(Pd-OTMM或Pd-NTMM)与环状或非环状1,3-二烯烃的催化不对称(3+2)环加成反应,通过C—N或C—O键形成终止反应路径,高效构建高取代或稠合的吡咯烷和四氢呋喃环(图7)[22]。该方法具有高效、操作简单、反应条件温和、化学选择性和对映选择性优异等显著特点,理性设计的PC-Phos配体在反应效率和选择性方面发挥了关键作用。突破了氧/氮杂烯丙基中间体仅可进行[4+3]和[2+1]环加成反应的限制,大大拓展了反应的类型。控制实验表明,杂烯丙基前体的顺/反构型与二烯烃存在明显的匹配/错配效应。结合手性催化剂PC6和产物的立体构型,提出了反应的手性诱导模型:PC-Phos作为O,P-手性配体,烯烃和酯部分与Pd(Ⅱ)中心配位,烯烃的Re面和酯部分被配体的3,5-二氟苯基手性柔性边臂屏蔽,因此1,3-二烯烃插入C—Pd键及分子内亲核攻击发生在Si面,形成顺式产物。
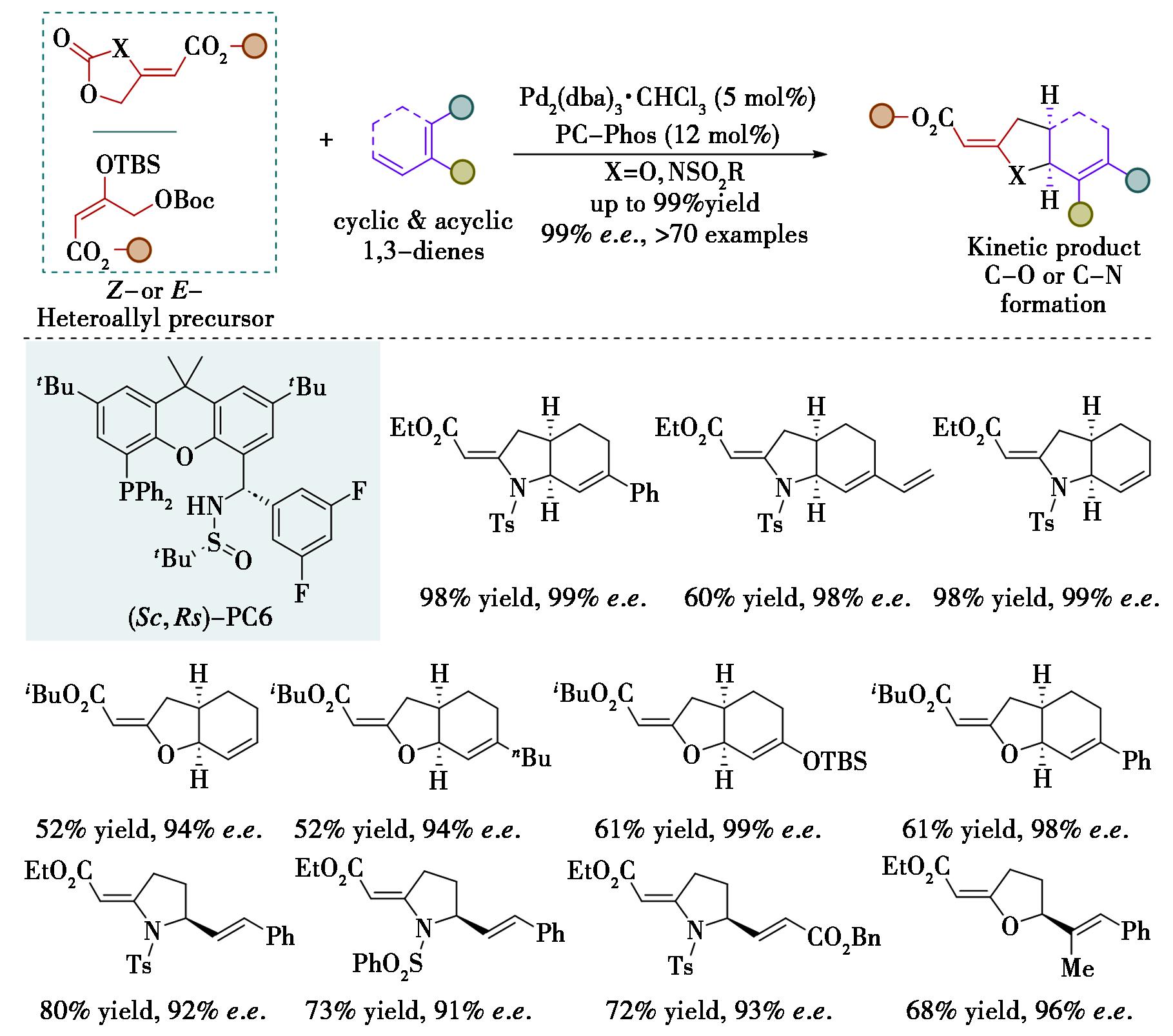
图7 PC-Phos促进的催化钯-杂烯丙基不对称环加成反应[22]
Fig.7 PC-Phos enabled catalytic Palladium-heteroallyl asymmetric cycloaddition[22]
过渡金属催化的不对称脱氮环加成反应是构建手性氮杂环的重要工具,但苯并三唑与不饱和烃的不对称脱氮环加成反应因苯并三唑开环生成α-亚胺金属卡宾物种的热力学不利性,长期以来研究极少。2019年,本课题组首次报道了Pd/PC-Phos催化的苯并三唑与联烯或联烯胺的不对称脱氮环化反应,为光学活性3-亚甲基吲哚啉的合成提供了高效方法(图8)[23]。分别利用含2-异丙基苯基和4-叔丁基苯基柔性边臂的PC-Phos,解决了产物区域选择性、联烯二聚化、配体与中间体兼容性及高对映选择性等挑战。此外,吲哚啉是多种生物活性单萜吲哚生物碱的核心骨架,其高效不对称合成具有重要价值。2021年,本课题组也首次报道了钯催化的苯并三唑与非环状1,3-二烯烃的不对称串联脱氮Heck/Tsuji-Trost反应,通过利用PC-Phos立体选择性调控,高效合成了一系列富含对映体的吲哚啉,解决了反应选择性控制和配体兼容性等关键问题。反应具有高效性、高对映选择性、操作简单、条件温和、官能团兼容性强等特点(图9)[24]。
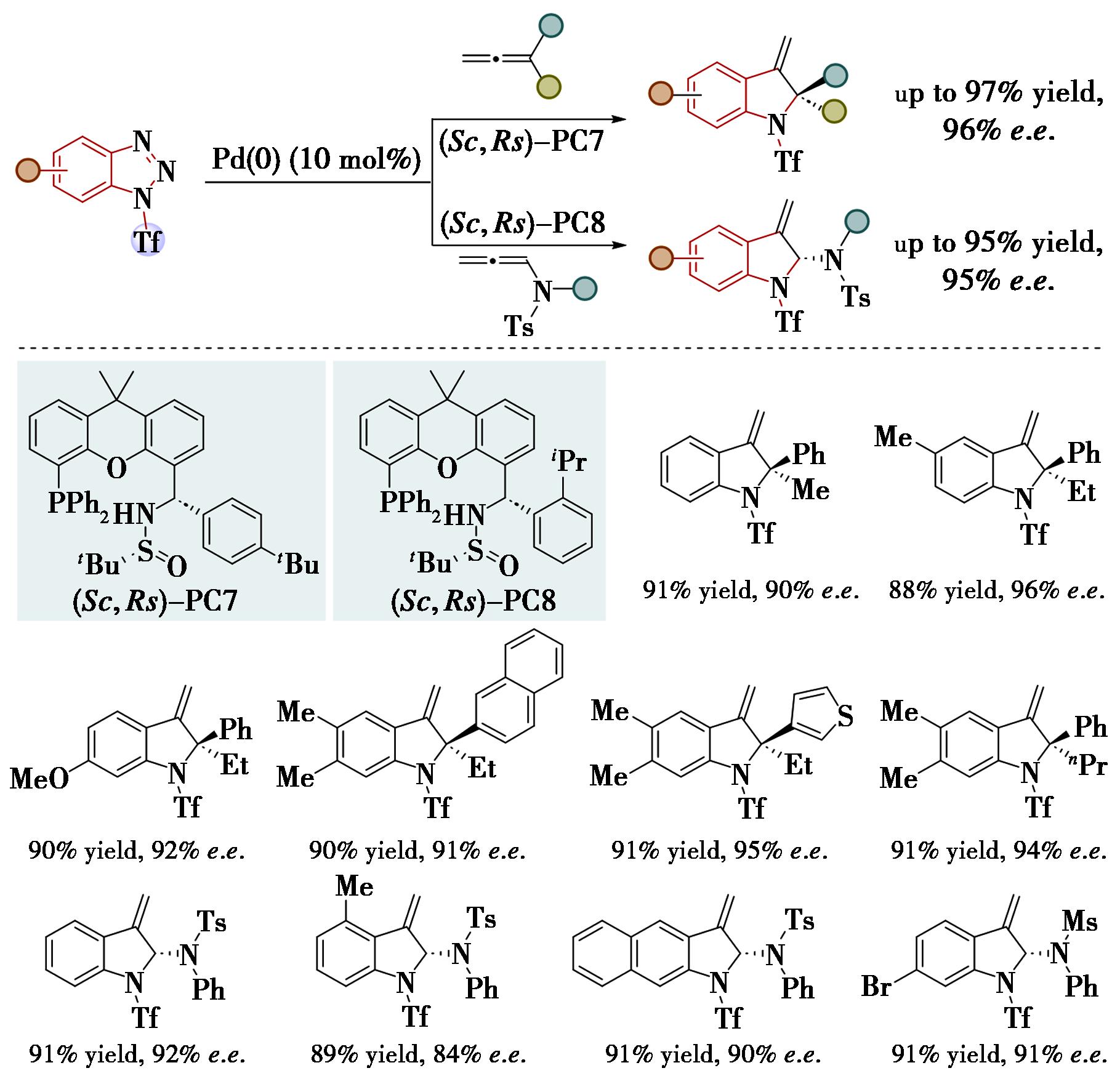
图8 Pd/PC-Phos催化的苯并三唑与联烯或联烯胺的不对称串联脱氮Heck/Tsuji-Trost反应[23]
Fig.8 Pd/PC-Phos catalyzed enantioselective domino denitrogenative Heck/Tsuji-Trost of benzotriazoles with allenes or N-allenamides[23]
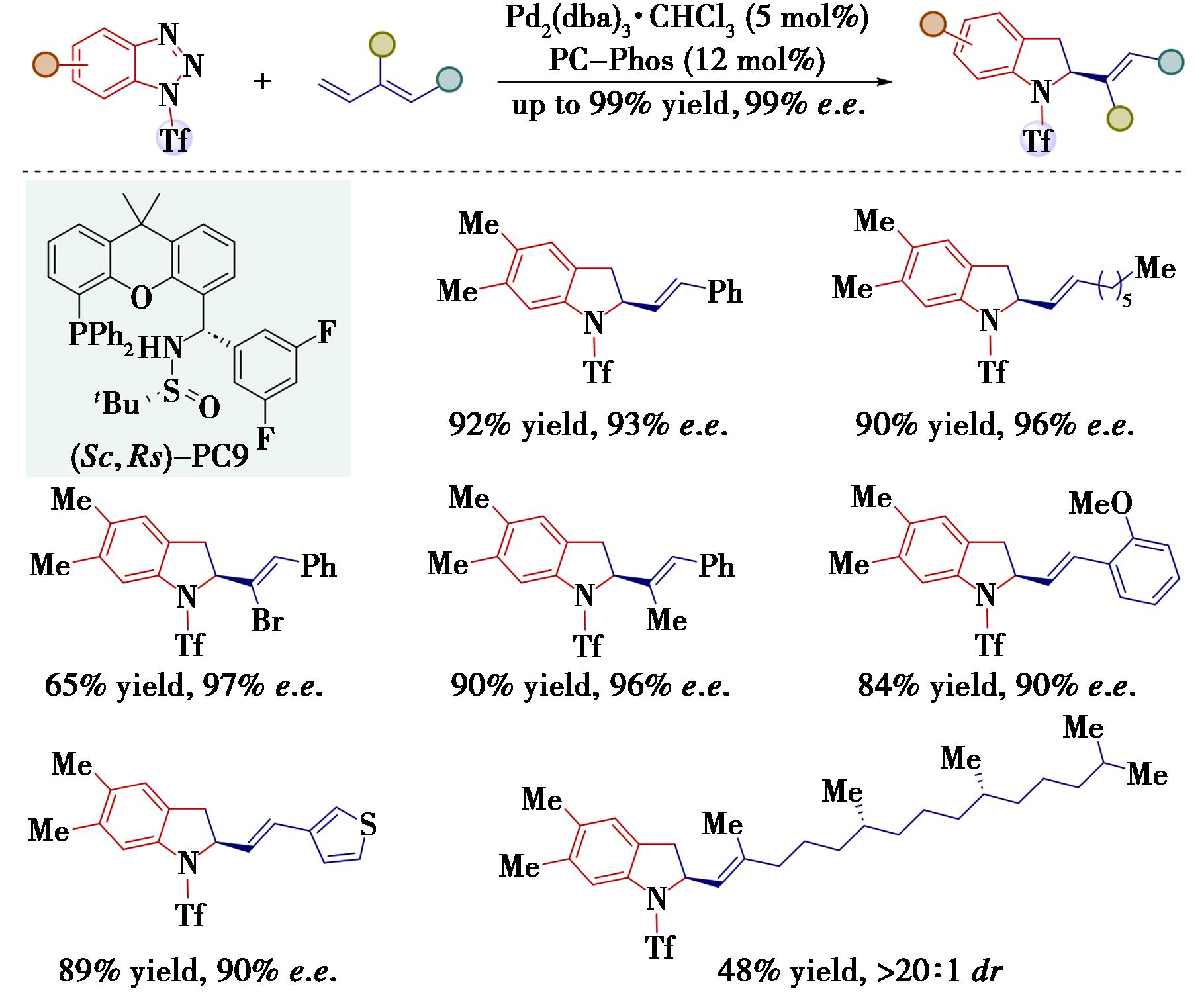
图9 Pd/PC-Phos催化的苯并三唑与1,3-二烯的不对称串联脱氮Heck/Tsuji-Trost反应[24]
Fig.9 Pd/PC-Phos catalyzed enantioselective domino denitrogenative Heck/Tsuji-Trost of benzotriazoles with 1,3-dienes[24]
六氢吲哚类化合物作为许多生物碱天然产物和治疗药物中的优势骨架,在不对称有机催化和天然产物合成中也具有重要价值。尽管已有一些合成外消旋六氢吲哚的方法,但从简单烯烃出发通过催化途径合成手性六氢吲哚仍是一个亟待解决的问题。2023年,本课题组首次报道了Pd/PC-Phos催化的氨基-1,3-环己二烯与芳基或烯基卤化物的不对称Heck/Tsuji-Trost反应,为高对映选择性和区域选择性合成功能化手性六氢吲哚提供了新方法,并将其应用于(-)-α-石蒜碱的简洁合成(图10)[25]。控制实验表明该串联反应存在匹配/错配问题。DFT计算表明,此形式1,2-反式碳胺化反应的催化循环过程中,氧化加成和配体交换均为放热过程,迁移插入是立体决定步骤,也是速率决定步骤。4-三氟甲基苯基作为PC-Phos配体的柔性手性边臂对实现优异的对映选择性至关重要。
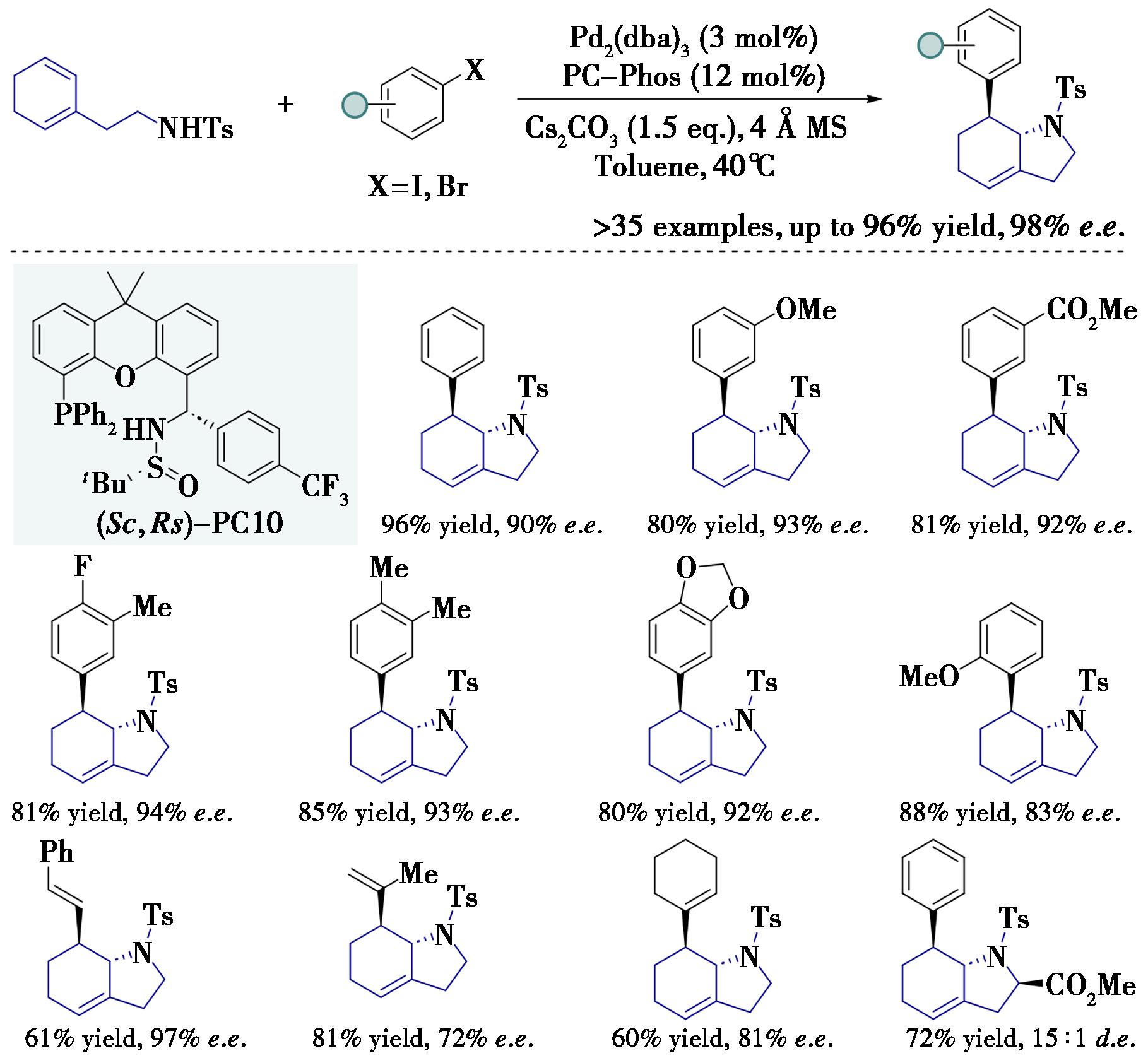
图10 Pd/PC-Phos催化的氨基-1,3-环己二烯与芳基或烯基卤化物的不对称串联Heck/Tsuji-Trost反应[25]
Fig.10 Palladium/PC-Phos-catalyzed asymmetric Heck/Tsuji-Trost reactions of amino-tethered 1,3-cyclohexadiene with aryl and alkenyl halides[25]
本文系统综述了2017~2025年氧杂蒽骨架手性亚磺酰胺膦配体PC-Phos在不对称催化中的创新应用。作为Sadphos配体家族的代表性成员,PC-Phos凭借其动态自适应特性与氧杂蒽骨架的结构优势,手性柔性边臂构建的精细可调的限域手性空间,以及和底物的非共价互相作用,共同提升了催化活性以及手性诱导能力。攻克了金催化Pictet-Spengler环化以及钯催化C—S/C—P偶联、Suzuki偶联、动力学拆分的去芳构化、钯杂烯丙基环加成和串联Heck/Tsuji-Trost反应等7类反应体系的一系列不对称催化难题。同时,PC-Phos的应用不仅为多种手性功能分子的高效合成提供了新途径,还为后续手性配体的设计与开发提供了宝贵的经验和思路。未来,需进一步探索其在历史性合成难题中的催化调控能力及工业化应用中的潜力。
[1]Dai L X,Lu X Y,Zhu G M.Chemistry,1995,6:15-22.
[2]Zhou Q L.Privileged Chiral Ligands and Catalysts.Germany:Wiley-VCH:Weinheim,2011.
[3]Liu Y Y,Li W B,Zhang J L.Natl.Sci.Rev.,2017,4:326-358.
[4]He Y M,Cheng Y Z,Duan Y D,Zhang Y D,Fan Q H,You S L,Luo S Z,Zhu S F,Fu X F,Zhou Q L.CCS Chem.,2023,5:2 685-2 716.
[5]Zhang Z M,Chen P,Li W B,Niu Y F,Zhao X L,Zhang J L.Angew.Chem.Int.Ed.,2014,53:4 350-4 354.
[6]Li W B,Zhang J L.Acc.Chem.Res.,2024,57:489-513.
[7]Hu H X,Wang Y D,Qian D Y,Zhang Z M,Liu L,Zhang J L.Org.Chem.Front.,2016,3:759-763.
[8]Zhang Z M,Xu B,Qian Y Y,Wu L Z,Wu Y Q,Zhou L J,Liu Y,Zhang J L.Angew.Chem.Int.Ed.,2018,57:10 373-10 377.
[9]Lin T Y,Pan Z J,Tu Y S,Zhu S,Wu H H,Liu Y,Li Z M,Zhang J L.Angew.Chem.,Int.Ed.,2020,59:22 957-22 962.
[10]Su X,Zhou W,Li Y Y,Zhang J L.Angew.Chem.Int.Ed.,2015,54:6 874-6 877.
[11]Wang Y D,Zhang P C,Di X Y,Dai Q,Zhang Z M,Zhang J L.Angew.Chem.Int.Ed.,2017,56:15 905-15 909.
[12]Han J,Zhou W,Zhang P C,Wang H M,Zhang R H,Wu H H,Zhang J L.ACS Catal.,2019,9:6 890-6 895.
[13]Qiu H L,Chen X F,Zhang J L.Chem.Sci.,2019,10:10 510-10 515.
[14]Zhao G F,Wu Y,Wu H H,Yang J F,Zhang J L.J.Am.Chem.Soc.,2021,143:17 983-17 988.
[15]Zhou W,Su X,Tao M,Zhu C Z,Zhao Q J,Zhang J L.Angew.Chem.Int.Ed.,2015,54:14 853-14 857.
[16]Leeuwen P W N M V,Kamer P C J.Catal.Sci.Technol.,2018,8:26-113.
[17]Leeuwen P W N M V,Cano I,Freixa Z.Coord.Chem.Rev.,2025,537:216 636.
[18]Wang L,Chen M J,Zhang P C,Li W B,Zhang J L.J.Am.Chem.Soc.,2018,140:3 467-3 473.
[19]Ma C,Wang X Y,Soós T,Zhang J L,Yang J F.Nat.Commun.,2025,16:5 436.
[20]Luan T R,Sun C,Tian Y L,Jiang Y K,Xi L L,Liu R R.Nat.Commun.,2025,16:2 370.
[21]Chu H K,Cheng J,Yang J F,Guo Y L,Zhang J L.Angew.Chem.Int.Ed.,2020,59:21 991-21 996.
[22]Zhang W G,Zhang P C,Li Y L,Wu H H,Zhang J L.J.Am.Chem.Soc.,2022,144:19 627-19 634.
[23]Zhang P C,Han J,Zhang J L.Angew.Chem.Int.Ed.,2019,58:11 444-11 448.
[24]Li Y L,Zhang P C,Wu H H,Zhang J L.J.Am.Chem.Soc.,2021,143:13 010-13 015.
[25]Feng J,Shi J Y,Wei L,Liu M Q,Li Z M,Xiao Y J,Zhang J L.Angew.Chem.Int.Ed.,2023,62:e202 215 407.