DOI:10.16445/j.cnki.1000-2340.20250314.002
中图分类号:S182;|X705
刘培蕾1, 孙燕1, 张继冉1, 徐淑霞1, 张世敏1, 马琳静2, 田甜甜1,3
| 【作者机构】 | 1河南农业大学生命科学学院; 2南阳市科学院; 3河南农业大学林学院 |
| 【分 类 号】 | S182;X705 |
| 【基 金】 | 国家重点研发计划项目(2021YFD1700900) 河南省自然科学基金青年基金项目(242300420335) 河南农业大学高层次人才专项支持基金项目(30501469) |
园林废弃物主要是指植物自然凋落或人工修剪所产生的枯枝、落叶、树木与灌木剪枝及其他植物残体等,也被称为园林垃圾或绿色垃圾,其成分90%以上是木质纤维素。木质纤维素主要包括木质素、纤维素和半纤维素,其中,木质素嵌入纤维素和半纤维素结构之间,形成复杂的网状结构,限制了微生物对纤维素和半纤维素的降解利用[1]。木质素是环境微生物降解园林废弃物的主要阻碍,解决其降解困难已成为高效处理园林废弃物的关键。2015年,中国正式颁布了GB/T 31755—2015《绿化植物废弃物处置和应用技术规程》[2],提出使用微生物菌剂可加快堆肥腐熟。微生物菌剂不仅能促进木质素和纤维素降解[3-4],还能起到固氮、解磷、解钾、生防和促生等作用[5-6]。
近年来,关于单菌株降解木质纤维素的研究较多,目前已经分离到可降解木质纤维素的细菌、真 菌200余 种[7]。其 中,真 菌 主 要 包 括 木 霉 属(Trichoderma sp.)、青霉属(Penicillium sp.)和曲霉属(Aspergillus sp.),细菌主要为芽孢杆菌属(Bacillus sp.)[8]。韩宇杰[9]从秸秆还田土壤中筛选出的3株细菌菌株,经过优化后木质素降解率分别达到16.72%、18.01%和21.65%。然而,单菌株产酶单一,难以突破木质素的网状“屏障”,使得降解酶不能直接接触纤维素,分解效果较差。鉴于此,众多学者将目光投向复合菌剂,期望借此提升木质纤维素的降解效率。付冰妍等[10-11]利用2株芽孢杆菌构建复合菌剂进行固态发酵试验,经过28 d的发酵后园林废弃物的木质素降解率最高为21.74%。余克非[12]研究发现,2株芽孢杆菌属细菌和1株曲霉属真菌组成的复合菌剂,经堆肥应用后堆体中木质素降解率达25.47%,相比对照组提高了10.37%。上述研究表明,在堆肥过程中添加园林废弃物复合菌剂可以提高木质素降解率,但是,在实际堆肥应用或实验室固态发酵试验中,木质素降解率仍然不高,园林废弃物实际堆肥生产效率受到极大限制。因此,筛选木质素高效降解菌并开发高效复合菌剂对于园林废弃物的堆肥处理至关重要。本研究从园林废弃物现场堆肥中分别筛选了木质素高效降解细菌和真菌,利用高效降解菌株复配木质素降解菌剂,并验证其木质素降解效果,以期为提高园林废弃物的堆肥效率提供科学基础。
样品采集:从郑州市植物园采集园林废弃物好氧堆肥样品,用于开展木质素高效降解菌的分离筛选;使用生物处理法对园林废弃物进行堆肥处理,堆肥物料包括枯枝、人工修剪的树木、灌木剪枝及少量落叶,粉碎程度保持均一,粉碎后物料粒径小于1.5 cm,颗粒状,堆肥物料量为1 000 kg;处理过程中含水量保持在40%~50%,堆体底部直径约1.2 m、高约1.0 m,于通风处自然堆置。
固态发酵试验材料:园林废弃物物料包括枯枝、人工修剪的树木、灌木剪枝及少量落叶。将物料进行粉碎,粉碎程度保持均一,粉碎后物料粒径为小于1.0 cm的颗粒状,高压灭菌,105 ℃烘干备用。
木质素降解培养基:碱性木质素2.0 g,磷酸二氢钾1.0 g,七水合硫酸镁1.0 g,蛋白胨1.0 g,补充蒸馏水至1 000 mL。121 ℃灭菌30 min。LB液体培养基:酵母浸粉5.0 g,蛋白胨10.0 g,氯化钠10.0 g,补充蒸馏水至1 000 mL。调节pH值7.2~7.4,121 ℃灭菌30 min。LB斜面培养基:酵母浸粉5.0 g,蛋白胨10.0 g,氯化钠10.0 g,琼脂粉20.0 g,补充蒸馏水至1 000 mL。pH值7.2~7.4。121 ℃灭菌30 min。马铃薯葡萄糖琼脂培养基(PDA培养基):称取200.0 g马铃薯,切成小块加水煮烂,纱布过滤后取滤液,继续加热,加入20.0 g葡萄糖,20.0 g琼脂粉搅拌溶解后,补充蒸馏水至1 000 mL。115 ℃灭菌30 min。马铃薯葡萄糖培养基(PDW培养基):称取200.0 g马铃薯,切成小块加水煮烂,纱布过滤后取滤液,继续加热,加入20.0 g葡萄糖搅拌溶解后,补充蒸馏水至1 000 mL。115 ℃灭菌30 min。PDA-苯胺蓝培养基:苯胺蓝100 mg,PDA培养基100 mL。115 ℃灭菌30 min。发酵产酶培养基:蛋白胨10.0 g,木质素磺酸钠5.0 g,牛肉膏5.0 g,氯 化 钠5.0 g,补 充 蒸 馏 水 至1 000 mL,pH值6.5~7.0。121 ℃灭菌30 min。
MQL-61R立式全温振荡培养箱(上海旻泉仪器 有 限 公 司);Arktik Thermal Cycler PCR仪(Thermo scientific公司);DH-500A电热恒温培养箱(北京中兴伟业仪器有限公司);FA2204电子天平(上海方瑞仪器有限公司);HH-8型电热恒温水浴锅(上海力辰邦西仪器科技有限公司);TGL-20B型高速离心机(上海安亭科学仪器厂);PHS-3C pH计(上海仪电科学仪器股份有限公司);Varioskan LUX多功能酶标仪(赛默飞世尔科技公司);EX30光学显微镜(宁波舞宇仪器有限公司)。
1.4.1 木质素高效降解菌株的筛选 菌株的初筛:从园林废弃物堆肥样品中取1.0 g置于无菌玻璃试管中,加9.0 mL无菌水混匀,梯度稀释至10-3、10-4、10-5,分别吸取100 μL稀释液涂布至木质素降解培养基中,置于37 ℃条件下恒温培养48 h,选取不同形态的菌株进行分离纯化,将纯化后的菌株接种于LB斜面培养基或PDA斜面培养基上,保存于4 ℃冰箱[13-14]。
菌株的复筛:挑取斜面上的单菌落,点接在PDA-苯胺蓝培养基上,样品分离出的细菌置于37 ℃、真菌置于30 ℃恒温培养48 h。圈径比(褪色圈半径R与菌落半径r的比值)R/r>1.5的菌株被认为是木质素高效降解菌。
1.4.2 木质素高效降解菌株的鉴定 形态学鉴定:对细菌进行生理生化鉴定和形态学鉴定,平板划线长出单菌落后观察其形状、颜色、大小、边缘、表面等形态特征,并进行革兰氏染色;对分离到的真菌进行形态学观察和鉴定,平板划线长出菌丝后,挑取菌丝于载玻片上,在40倍显微镜下观察。
分子生物学鉴定:对于细菌,使用Fast Pure Bacteria DNA Isolation Mini Kit (南京诺唯赞生物科技股份有限公司)提取细菌基因组DNA。对于真菌,将斜面培养基上的菌丝挑取至研钵中,加入液氮研磨直至菌丝破碎且颜色变深,使用Fast Pure Plant DNA Isolation Mini Kit 50rxns(南京诺唯赞生物科技股份有限公司)提取真菌基因组DNA。
参照杨趁仙[15]的方法对细菌菌株进行16S rDNA的 PCR扩增;参照白长胜等[16]的方法对真菌菌株进行ITS PCR扩增。PCR产物经质量分数1%琼脂糖凝胶电泳检测后,细菌PCR扩增片段长度约为1 500 bp、真菌PCR扩增片段长度约为750 bp,符合要求的将PCR原液送至北京擎科生物科技股份有限公司进行测序,测序结果提交NCBI(https://blast.ncbi.nlm.nih.gov/Blast.cgi)进 行 序列比对,结合形态学鉴定及生理生化鉴定确定分离菌株的种属。
1.4.3 木质素降解菌剂的制备 从1.4.1筛选出的木质素高效降解菌中,挑选各细菌分别接种至300 mL LB液体培 养 基 中,在37 ℃、180 r·min-1振荡培养1~2 d,直至菌液中活菌数达到2×108 CFU·mL-1;挑取各真菌菌丝和孢子分别接种至200 mL PDW培养基中,30 ℃、200 r·min-1振荡培养5 d,使菌丝球长满整个液体培养基。将各细菌培养液按照等体积比例混合后构建菌剂M01;将各真菌培养液按照等体积混合后构建菌剂M02;将所有培养液按照等体积混合后构建菌剂M03[17]。
1.4.4 单菌及木质素降解菌剂的酶活力测定 分别接种体积分数5%的单菌细菌菌液、单菌真菌菌液和3种菌剂于发酵产酶培养基中,置于30 ℃、180 r·min-1培养3 d,取发酵液于4 ℃、12 000 r·min-1离心10 min,取上清液作为粗酶液[12]。
漆酶酶活力测定及计算参照田林双[18]和WOLFENDEN等[19]的 方法;木质素过氧化物酶酶活力的测定及计算参照田林双[18]和WARIISHI等[20]的方法;锰过氧化物酶酶活力测定及计算参照田林双[18]和TIEN等[21]的方法。
1.4.5 木质素降解菌剂的固态发酵试验 对照组CK及3个处理组T1、T2、T3按表1所示组成成分进行固态发酵试验。于37 ℃条件下发酵15 d,验证菌剂对木质素的降解能力,即物料质量损失率和木质素降解率。15 d后取发酵物料烘干至恒质量,测定发酵物料干质量,按式(1)计算物料质量损失率;采用Vansoest酸性洗涤法测定发酵前后木质素干质量,按式(2)计算木质素降解率[22]。
表1 3 种木质素降解菌剂的固态发酵试验设计
Table 1 Experimental design of solid-state fermentation of three kinds of microorganism agents.

处理Treatment CK T1 T2 T3物料添加质量/g Material addition mass 400 400 400 400试剂添加种类Reagent agents addition category生理盐水M01 菌剂M02 菌剂M03 菌剂添加体积/mL Volumes of agents addition 400 400 400 400
式中:Y1为质量损 失率;m1为发酵 前干质量;m2为发酵后干质量;Y2为木质素降解率;m3为发酵前木质素干质量;m4为发酵后木质素干质量。
所得数据采用Microsoft Excel 365进行初步分析,利用Prism进行差异显著性分析和作图,p<0.05表示在统计学意义上差异显著。
从园林废弃物堆肥中共筛选出31株具有形态学差异的木质素降解菌,包括21株细菌和10株真菌。21株细菌菌落多数呈圆形,湿润有光泽,颜色不透明,经革兰氏染色后显微镜下均呈紫色,判断为革兰氏阳性菌,且细胞多呈直杆状或弯曲的棒状。10株真菌中,1株菌的菌落呈深黄绿色,反面呈不同程度黄色,显微镜下观察分生孢子链状着生,呈球形,分生孢子梗呈扫帚状分枝,判断为青霉属;1株菌的菌落呈蓝绿色,边缘稍有白色,老后呈现同心环纹,显微镜下观察分生孢子球形,绿色,孢子梗表面粗糙,可能为篮状菌;其余8株真菌经显微镜观察其具有顶囊、瓶梗、梗基和分生孢子链组成的分生孢子头,具有足细胞,由分生孢子梗连接顶囊和足细胞,判断8株菌属于曲霉属真菌。
利用PDA-苯胺蓝培养基对其进行复筛,分子生物学鉴定的测序结果在NCBI Blast中进行比对,综合菌株的形态学及16S rDNA、ITS基因序列的分析结果,去除重复菌株中褪色圈小的菌株,最后共得到6株细菌和7株真菌,如图1和图2所示。在MEGA 7.0软件中采用似然法构建系统发育树,如图3和图4。经鉴定,6株细菌分别为解淀粉芽孢杆菌Bacillus amyloliquefaciens (PP527002)、地衣芽孢杆菌Bacillus licheniformis (PP527005)、栗褐芽孢杆 菌Bacillus badius (PP527006)、枯 草 芽 孢 杆 菌Bacillus subtilis (PP527008)、蜡样芽孢杆菌Bacillus cereus (PP532709)、特基拉芽孢杆菌Bacillus tequilensis (PP532710);7株真菌分别为黄曲霉Aspergillus flavus (PP534994)、草酸青霉Penicillium oxalicum(PP534997)、黑曲霉Aspergillus niger (PP535009)、烟曲霉Aspergillus Fumigatus (PP535015)、篮状菌Talaromyces funiculosus (PP534995)、胡椒曲霉Aspergillus piperis (PP535013)、米 曲 霉Aspergillus oryzae(PP535010)。括号内为Gen Bank号。

图1 园林废弃物木质素高效降解真菌菌落特征
Fig.1 Colony characteristics of highly efficient lignindegrading fungi screened from garden waste

图2 园林废弃物木质素高效降解细菌苯胺蓝褪色反应
Fig.2 Aniline blue fading reaction of highly efficient lignin-degrading bacteria screened from garden waste

图3 园林废弃物木质素高效降解真菌系统发育树
Fig.3 Phylogenetic tree of highly efficient lignin-degrading fungi screened from garden waste

图4 园林废弃物木质素高效降解细菌系统发育树
Fig.4 Phylogenetic tree of highly efficient lignin-degrading bacteria screened from garden waste
将筛选出的木质素高效降解菌按照1.4.3的方法制备木质素降解菌剂M01、M02、M03。其中,M01包含6种细菌培养液,颜色为淡黄色,较为浑浊;M02包含7种真菌培养液,颜色为深黄色,透明,有大量白色和黄色的小球状漂浮物;M03包含6种细菌培养液和7种真菌培养液,颜色为深黄色,轻微浑浊,有大量小球状漂浮物。
木质素高效降解菌株单菌和3种降解菌剂的酶活力及差异显著性分析如表2所示。其中,漆酶酶活力最低的是米曲霉PP535010,为104.0 U·L-1,最高的是胡椒曲霉PP535013,达1 102.8 U·L-1。与单一菌株相比,由混菌构建的3种木质素降解菌剂的漆酶酶活力均有显著提高,且菌剂M03最高,达1 495.4 U·L-1,比胡椒曲霉提升了35.7%。黑曲霉PP535009的木质素过氧化物酶酶活力最高,达到2 568.4 U·L-1;与单一菌株相比,木质素降解菌剂M02和M03的酶活力有显著提升,分别为3 660.0和8 548.8 U·L-1,其中,菌剂M03的酶活力比黑曲霉提高了89.4%。与漆酶、木质素过氧化物酶酶活力相似,木质素降解菌剂M03的锰过氧化物酶酶活力与单一菌株相比有显著提高,达到6 092.6 U·L-1,比单菌株中酶活力最高的烟曲霉提高了70.9%。上述研究表明,木质素降解菌剂M03在实验室条件下产酶能力最好。
表2 木质素降解菌株单菌及3 种菌剂中漆酶、木质素过氧化物酶、锰过氧化物酶的酶活力
Table 2 Enzyme activities of laccase,lignin peroxidase and manganese peroxidase in individual lignin degrading strain and three kinds of compound microbial agents

注:同列不同字母表示在统计学意义上差异显著(p<0.05)。
Note:Different letters in the same column indicate statistically significant differences (p<0.05).
组别Category PP534994 PP534997 PP535009 PP535015 PP534995 PP535013 PP535010 PP527002 PP527005 PP527006 PP527008 PP532709 PP532710 M01 M02 M03锰过氧化物酶酶活力/(U·L-1)Manganesen peroxidases enzyme activity 1 061.6±47.9 ef 1 617.7±42.2 b 1 769.9±28.0 bc 3 565.3±97.3 cd 1 104.7±88.6 a 740.3±97.3 a 817.8±60.2 a 1 230.7±16.2 a 2 339.8±56.1 b 1 526.1±43.2 ab 1 800.8±62.8 b 1 683.0±125.9 a 983.0±25.9 a 4 431.0±118.4 de 2 639.0±148.4 fg 6 092.6±159.3 h漆酶酶活力/(U·L-1)Laccases enzyme activity 209.3±6.2 a 206.3±5.0 a 549.2±9.2 c 423.6±16.2 c 310.9±24.6 ab 1 102.8±7.3 d 104.0±5.8 a 504.0±16.2 bc 411.2±87.0 c 335.1±34.0 c 638.6±77.0 cd 349.2±91.0 c 127.4±18.0 a 1 358.8±83.2 e 1 200.8±24.9 de 1 495.4±20.2 e木质素过氧化物酶酶活力/(U·L-1)Lignin peroxidases enzyme activity 1 737.4±46.7 a 2 735.9±21.4 d 2 568.4±59.3 g 1 427.1±25.5 fg 2 937.4±17.4 eg 1 437.6±15.5 c 3 527.1±25.5 b 2 146.6±69.8 ab 3 204.3±10.1 bc 1 758.6±45.1 cd 4 514.0±32.2 b 1 705.9±13.9 g 2 102.3±11.8 de 6 582.9±130.0 gh 3 660.0±44.0 ij 8 548.8±177.2 j
通过固态发酵试验验证木质素降解菌剂对园林废弃物的处理效果。不同处理对园林废弃物的物料质量损失率和木质素降解率的影响如图5所示。经过15 d的发酵后,试验组T1、T2、T3的物料质量损失率分别为40.75%、44.75%、56.25%,与对照组13.25%相比有显著提升。其中,试验组T3质量损失率最高,比对照组CK提高了约4倍。发酵前4组木质素初始干质量分别为135.3、135.1、135.6、135.4 g。试验组中T1对木质素的降解率最低,为31.10%;T2对木质素降解率为35.54%;T3最高,达到52.95%。相比对照组的5.10%,试验组T3的木质素降解率提高了约10倍。这表明,与酶活力测定结果相似,试验组T3在固态发酵试验中效果最好,即菌剂M03在实验室条件下对园林废弃物中的木质素降解效果最好。
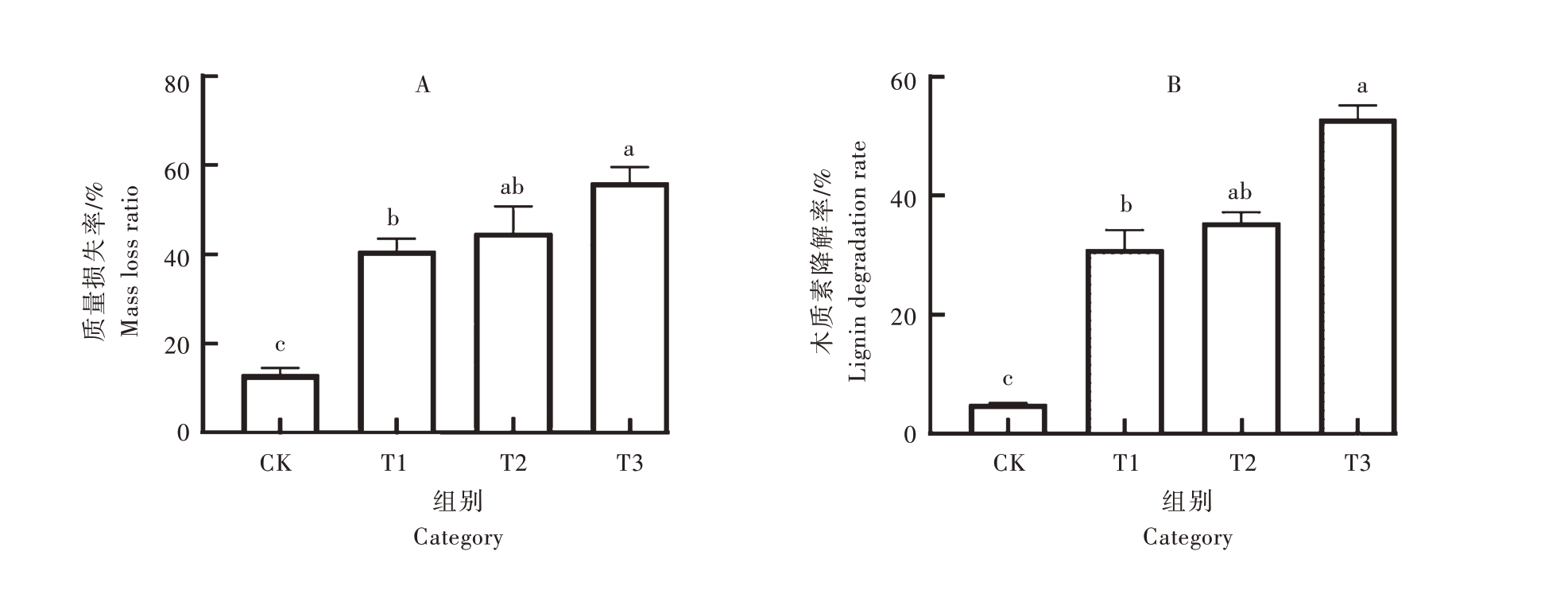
图5 固态发酵试验中木质素降解菌剂对园林废弃物的处理效果
Fig.5 The effect of lignin-degrading bacterial agents on garden waste treatment in solid-state fermentation experiments
A 为固态发酵试验中园林废弃物的质量损失率;B 为固态发酵试验中园林废弃物中木质素的降解率。不同小写字母表示在统计学意义上差异显著(p<0.05)。
A means the mass loss rates of garden waste in solid-state fermentation tests;B means the degradation rates of lignin in garden waste in solid-state fermentation tests.Different lowercase letters indicate statistically significant differences (p<0.05).
堆肥处理可以将植物残体去木质化,将有机物转化为肥料,有利于增加土壤肥力,促进园林废弃物的资源化利用[23-24]。在堆肥过程中添加微生物菌剂有利于降解木质素,且与单一菌株接种相比,混合菌剂接种可显著提高木质素的降解率[25]。本研究从园林废弃物堆肥过程中筛选了13株木质素高效降解菌,包括6株芽孢杆菌属细菌、5株曲霉属真菌及1株草酸青霉和1株篮状菌。在此基础上,本研究配制出了3种木质素降解菌剂,分别为M01、M02、M03。酶活力测定和固态发酵试验验证表明,菌剂M03在实验室条件下的木质素降解酶酶活力最高,漆酶、木质素过氧化物酶、锰过氧化物酶的酶活力分别达到1 495.4、8 548.8、6 092.6 U·L-1,对园林废弃物中的木质素的降解效果最好,质量损失率达到56.25%,木质素降解率达到52.95%。
目前,针对降解木质素的微生物种类及其降解机制已有广泛研究,发现不同菌株对木质素的降解能力存在显著差异[26-27]。据报道,芽孢杆菌属等细菌可产生漆酶,打开芳香环,破坏烷基-芳基增加酚羟基,促进木质素分子的裂解[10];曲霉属等真菌能够降解果胶、纤维素等,并通过产生木质素过氧化物酶和锰过氧化物酶裂解木质素结构中Cα-Cβ化学键及氧化侧链和催化苯环裂解,将木质素解聚生成二芳基丙烷和芳基醚等低聚体,从而降解木质素[28-29]。已有研究表明,将木质素降解菌制备为菌剂可有效提升木质素降解率。孟童瑶[30]将1株曲霉属真菌制备为固体菌剂并进行为期40 d的固态发酵试验,木质素降解率为46.65%。MEI等[31]研究发现,与未接种堆肥物料相比,在烟草秸秆堆肥中接种木质素降解菌解淀粉芽孢杆菌SL-7,木质素降解率提高22.26%。YADAV等[32]从污泥中筛选得到的枯草芽孢杆菌和肺炎克雷伯菌对牛皮纸木质素的降解率分别为39%和44%,将其联合培养后降解率得到有效提升。王炳坤[33]的研究表明,JA复合菌剂(包含3株真菌Z6、Z14、Z17和1株细菌X20)的综合产酶能力最高,其产漆酶的能力最强,秸秆降解率较高,秸秆纤维素、半纤维素、木质素降解率均较高。与前人开发的菌剂相比,本研究开发的复合菌剂M03中包含了6种细菌和7种真菌,菌株种类更丰富,产酶能力更强,同时木质素降解效率可达52.95%,效果优于其他菌剂。上述结果与CHEN等[34]的研究相符,即微生物的种类和数量越多,降解效率越高。
综上所述,本研究从园林废弃物实际堆肥中筛选出了13株高效木质素降解菌,利用其复配了3种木质素降解菌剂M01、M02、M03,其中,木质素降解菌剂M03具有更高的木质素降解能力。本研究开发的微生物菌剂M03后续可通过调节菌种比例、优化发酵产酶条件等进一步提高其木质素降解效率。同时,可进一步将菌剂应用于现场堆肥试验,测定其对堆肥过程木质素降解和堆肥腐熟度的影响,以便更好地将其投入到实际生产应用中。
[1]李强,吴晓青,张新建.微生物降解秸秆木质素的研究进展[J].微生物学报,2023,63(11):4118-4132.LI Q,WU X Q,ZHANG X J.Research progress in microbial degradation of straw lignin[J].Acta Microbiologica Sinica,2023,63(11):4118-4132.
[2]国家质量监督检验检疫总局,中国国家标准化管理委员会.绿化植物废弃物处置和应用技术规程:GB/T 31755—2015[S].北京:中国标准出版社,2015.General Administration of Quality Supervision,Inspection and Quarantine of the People’s Republic of China,Standardization Administration of the People’s Republic of China.Technical regulation of disposal and application for greenery waste:GB/T 31755—2015[S].Beijing:Standards Press of China,2015.
[3]BOLDRIN A,ANDERSEN J K,CHRISTENSEN T H.Environmental assessment of garden waste management in the Municipality of Aarhus,Denmark[J].Waste Management,2011,31(7):1560-1569.
[4]张旭屹,彭仕乐,谢慧,等.固氮与秸秆降解复合菌剂构建及其在秸秆还田中的应用[J].河南农业大学学报,2025,59(2):306-315.ZHANG X Y,PENG S L,XIE H,et al.Construction of nitrogen fixation and straw degradation composite microbial agent and its application in straw returning to the field[J].Journal of Henan Agricultural University,2025,59(2):306-315.
[5]徐兰梦,袁岩聪,彭昕,等.复合菌制剂对麻羽肉鸡性能和肠道微生物的影响[J].西南大学学报(自然科学版),2024,46(5):87-98.XU L M,YUAN Y C,PENG X,et al.Effects of compound bacterial preparation on performance and gut microbiota of Mayu broilers[J].Journal of Southwest University (Natural Science Edition),2024,46(5):87-98.
[6]刘玲,冯乃杰,郑殿峰,等.不同微生物菌剂对水稻幼苗形态建成和生理特性的影响[J].南方农业学报,2022,53(1):88-95.LIU L,FENG N J,ZHENG D F,et al.Effects of different microbial agents on the morphogenesis and physiological characteristics of rice seedlings[J].Journal of Southern Agriculture,2022,53(1):88-95.
[7]才金玲,冯飞,李佳欣,等.木质素生物降解研究进展[J].应用化工,2024,53(7):1681-1686.CAI J L,FENG F,LI J X,et al.Research progress of biological decomposition lignin[J].Applied Chemical Industry,2024,53(7):1681-1686.
[8]宫秀杰,钱春荣,于洋,等.近年纤维素降解菌株筛选研究进展[J].纤维素科学与技术,2021,29(2):68-77.GONG X J,QIAN C R,YU Y,et al.Progress on screening of cellulose degrading strains in recent years[J].Journal of Cellulose Science and Technology,2021,29(2):68-77.
[9]韩宇杰.秸秆木质素降解菌株的筛选及其降解机理的研究[D].哈尔滨:中国科学院东北地理与农业生态研究所,2024.HAN Y J.Screening of straw lignin degrading strain and study on its degradation mechanism[D].Harbin:Northeast Institute of Geography and Agroecology,Chinese Academy of Sciences,2024.
[10]付冰妍,孙向阳,余克非,等.降解园林废弃物专用固体复合菌的构建及其堆肥效应研究[J].环境科学研究,2021,34(5):1231-1237.FU B Y,SUN X Y,YU K F,et al.Construction of solid composite inoculum for green waste degradation and its effect on composting[J].Research of Environmental Sciences,2021,34(5):1231-1237.
[11]付冰妍,孙向阳,余克非,等.芽孢杆菌B01 固态发酵及其对园林废弃物堆肥的影响[J].环境科学研究,2021,34(2):450-457.FU B Y,SUN X Y,YU K F,et al.Solid state fermentation of Bacillus sp.B01 and its effect on green waste composting[J].Research of Environmental Sciences,2021,34(2):450-457.
[12]余克非.园林绿化废弃物堆肥优势降解菌的筛选及复合菌剂配比研究[D].北京:北京林业大学,2020.YU K F.Screening of dominant degrading bacteria for composting landscaping waste and study on the proportion of compound fungi[D].Beijing:Beijing Forestry University,2020.
[13]黄秋月,何建清,刘海鑫,等.园林废弃物木质纤维素高效降解真菌的筛选与鉴定[J].河南农业科学,2024,53(5):101-111.HUANG Q Y,HE J Q,LIU H X,et al.Screening and identification of efficient degradation fungi for garden waste lignocellulose[J].Journal of Henan Agricultural Sciences,2024,53(5):101-111.
[14]李灵灵,王敬红,赵铎,等.木质素降解菌BYL-7 的筛选及降解条件优化[J].微生物学通报,2020,47(12):4059-4071.LI L L,WANG J H,ZHAO D,et al.Screening of lignin degrading strain BYL-7 and optimization of degradation conditions[J].Microbiology China,2020,47(12):4059-4071.
[15]杨趁仙.木质素降解细菌的筛选及其酶对木质素降解机制的研究[D].杨凌:西北农林科技大学,2018.YANG C X.Screening of lignin degrading bacteria and study on lignin degrading mechanism by enzymes [D].Yangling:Northwest A&F University,2018.
[16]白长胜,刘秋瑾,尹珺伊,等.产木质纤维素降解酶真菌的筛选及产酶特性[J].微生物学通报,2023,50(3):1098-1110.BAI C S,LIU Q J,YIN J Y,et al.Screening and enzymatic characterization of the fungal strains producing lignocellulose-degrading enzymes[J].Microbiology China,2023,50(3):1098-1110.
[17]李春黎,李文豪,余君,等.烟秆高效复合降解菌群的筛选、鉴定及组合应用[J].中国烟草科学,2019,40(6):26-32.LI C L,LI W H,YU J,et al.Screening,identification and combination of high efficiency degrading bacteria for tobacco stem[J].Chinese Tobacco Science,2019,40(6):26-32.
[18]田林双.木质素降解相关酶类测定标准方法研究[J].畜牧与饲料科学,2009,30(10):13-15.TIAN L S.Research on standard method for determining ligninolytic enzyme activity[J].Animal Husbandry and Feed Science,2009,30(10):13-15.
[19]WOLFENDEN B S,WILLSON R L.Radical-cations as reference chromogens in kinetic studies of onoelectron transfer reactions:pulse radiolysis studies of 2,2’- azinobis-(3-ethylbenzthiazoline-6-sulphonate)[J].J Chem Soc,Perkin Trans 2,1982(7):805-812.
[20]WARIISHI H,VALLI K,GOLD M H.Manganese(II)oxidation by manganese peroxidase from the basidiomycete Phanerochaete chrysosporium.Kinetic mechanism and role of chelators[J].Journal of Biological Chemistry,1992,267(33):23688-23695.
[21]TIEN M,KIRK T K.Lignin-degrading enzyme from Phanerochaete chrysosporium:purification,characterization,and catalytic properties of a unique H2O2 -requiring oxygenase[J].Proceedings of the National Academy of Sciences of the United States of America,1984,81(8):2280-2284.
[22]TSANG L J,REID I D,COXWORTH E C.Delignification of wheat straw by Pleurotus spp.under mushroomgrowing conditions[J].Applied and Environmental Microbiology,1987,53(6):1304-1306.
[23]刘瑞,张丽,孙鹏,等.微生物法降解木质素的研究进展[J].微生物学通报,2023,50(7):3232-3244.LIU R,ZHANG L,SUN P,et al.Microbial degradation of lignin:areview[J].Microbiology China,2023,50(7):3232-3244.
[24]田婧婕,崔二苹,刘春成,等.生物强化技术在农业废弃物堆肥处理中的应用及研究进展[J].河南农业科学,2024,53(11):1-16.TIAN J J,CUI E P,LIU C C,et al.Application status and research progress of bioaugmentation technology in agricultural waste composting treatment[J].Journal of Henan Agricultural Sciences,2024,53(11):1-16.
[25]杨文敏.黄孢原毛平革菌和康氏木霉联合降解园林废弃物及其应用[D].金华:浙江师范大学,2021.YANG W M.Degradation of garden waste by Phanerochaete chrysosporium and Trichoderma koningii and its application[D].Jinhua:Zhejiang Normal University,2021.
[26]王献鑫,祁丽桦,宋江富,等.纤维素、木质素降解菌的筛选及对菌渣堆肥的影响[J].河南农业科学,2024,53(9):66-79.WANG X X,QI L H,SONG J F,et al.Screening of cellulose and lignin degrading bacteria and their effect on composting of mushroom residue[J].Journal of Henan Agricultural Sciences,2024,53(9):66-79.
[27]沈丹青,于鑫,韩捷,等.芽孢杆菌固体菌剂对园林绿化废弃物堆肥的影响[J].西北农林科技大学学报(自然科学版),2024,52(1):127-135.SHEN D Q,YU X,HAN J,et al.Effect of Bacillus solid bacterial inocula on compost of green waste[J].Journal of Northwest A&F University (Natural Science Edition),2024,52(1):127-135.
[28]李婕,李敏,汪玲玲,等.高产纤维素酶真菌的筛选鉴定与紫外诱变选育研究[J].饲料研究,2023,46(17):76-81.LI J,LI M,WANG L L,et al.Screening,identification and breeding of high-yielding cellulase fungi by UV mutation[J].Journal of Feed Research,2023,46(17):76-81.
[29]李金达.基于蛋白质组学和代谢组学的烟曲霉G:13木质素降解机理研究[D].哈尔滨:哈尔滨理工大学,2020.LI J D.Study on lignin degradation mechanism of Aspergillus fumigatus G:13 based on protein metabonomics and metabonomics[D].Harbin:Harbin University of Science and Technology,2020.
[30]孟童瑶.园林绿化废弃物堆肥木质素、纤维素降解固体菌剂的研制及应用[D].北京:北京林业大学,2021.MENG T Y.Development and application of solid microbial inoculum for lignin and cellulose degradation in landscaping waste compost[D].Beijing:Beijing Forestry University,2021.
[31]MEI J F,SHEN X B,GANG L P,et al.A novel lignin degradation bacteria-Bacillus amyloliquefaciens SL-7 used to degrade straw lignin efficiently[J].Bioresource Technology,2020,310:123445.
[32]YADAV S,CHANDRA R.Syntrophic co-culture of Bacillus subtilis and Klebsiella pneumonia for degradation of kraft lignin discharged from rayon grade pulp industry[J].Journal of Environmental Sciences,2015,33:229-238.
[33]王炳坤.玉米秸秆低温降解菌复合菌剂制备及应用效果研究[D].长春:吉林农业大学,2022.WANG B K.Study on preparation and application effect of corn stalk low temperature degrading bacteria compound microbial inoculum[D].Changchun:Jilin Agricultural University,2022.
[34]CHEN X M,CHENG W T,LI S Z,et al.The quality and quantity of microbial species drive the degradation of cellulose during composting[J].Bioresource Technology,2021,320:124425.
Isolation and identification of highly efficient lignin-degrading microorganisms from garden waste and development of microorganism agents

X